原标题:你想了解创新药的问题都在里面来源:老罗话指数投资
整理了大家最关心的关于创新药的问题,并做了对应的解答,供大家参考。
1
创新药行业概况
问题一
什么是创新药?
答:在国际上,创新药一般指新的化学实体或者生物制品中新的物质。就国内而言,创新药是指在境内外均未上市的、含有新的结构明确的、具有药理作用的化合物,且具有临床价值的药品。
创新药行业产业链主要由上游创新药医药原材料生产商、中游创新药生产及销售企业、下游医疗机构等创新药销售终端组成。
问题二
创新药行业有什么特点?
答:创新药行业主要有研发周期长、投入较大的特点。一般情况下,创新药从研发至上市需要花费10年左右时间,主要经历:
(1)临床前研究阶段(2-3年):新药实体的发现与确立;
(2)临床前实验阶段(2-4年):安全性有效性测验;
(3)临床试验阶段(3-7年):I、II、III期临床;
(4)创新药上市审批阶段(半年):新药申请;
(5)上市后监测:多次审查。
在此过程中,创新药企业需要投入大量的人力、物力成本。这样的特性造就了创新药行业龙头企业竞争优势显著的特征。
问题三
海外创新药行业的发展轨迹如何,对我们有何启示?
答:从发展轨迹来看,我国当前医药行业变迁和日本上世纪末的情况类似:
(1)人口结构方面,日本老年人口从1980年的不足9%在15年时间内飙升至1995年的15%,目前我国人口老龄化率已逼近日本当时的水平;
(2)医保制度方面,日本与我国实行的都是全民医保制度,因此日本当时也面临着如今我国面临的人口老龄化带来的医保费用压力;
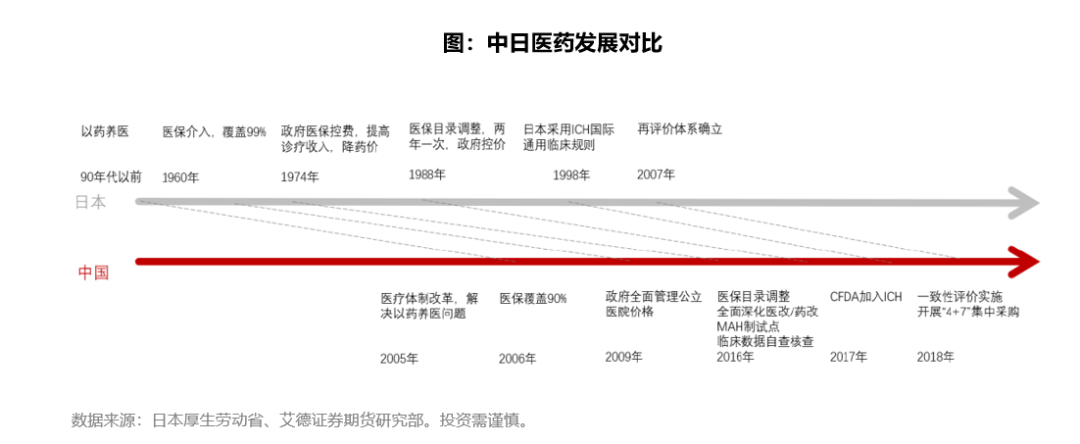
(3)日本和中国在医药方面政策同样经历了以药养医、医保介入、药价改革、仿制药再评价、目录调整等阶段。
综合考虑老龄化情况、医保体系、市场结构、研发水平、社会文化等方面,总体而言,中日两国医药行业发展轨迹高度相似,前后进程相差约20年,为此我们参照日本创新药企业的崛起和现状,来为研究我国创新药未来的发展提供参考。
20世纪70年代,日本基本实现了全民医保,医疗费用支出不断增加。20世纪90年代开始,日本经济增速开始步入下行,随后日本人口结构出现老龄化,医保费用支出的压力逐步加重,社会保障制度受到威胁,厚生劳动省开始通过多途径开始削减医疗支出,并推动创新药的发展。
(1)定期调整医保目录药品价格:由于日本几乎所有的药品都列入了医保目录,因此政府对于药品价格具有一定的定价权。从1980年开始,日本药价平均每年下降约4%至10%。
(2)扶持国产药企进行药品国产化替代:早期研发实力有限,日本药品以进口为主,价格较高,为此政府通过了“保姆政策”支持日本药企研发生产“本土化”品种,推动日本药企竞争Me-Too ,提高原研药的替代率,降低日本医药市场的药价水平,在此过程中提高了药企的研发实力,缩短了与欧美之间的差距。
(3)推行仿制药再评价:与中国一致性评价相似,日本2007年完成再评价体系,通过政府背书保障仿制药在安全性和有效性上与原研一致。该政策使得大量中小规模药企生存空间压缩,仿制药市场向头部集中。仿制药品降价叠加当时日本经济步入衰退期,药企纷纷开始转型研发创新发展。同期政府通过一系列政策支持国产创新药走出海外等方式,为药企打开了研发创新的黄金期。
2018年,日本制药市场规模约867亿美元,排全球第四。日本2018年仿制/首仿药占所有处方药数量占90%,而创新原研药占10%,但以销售额计算,仿制药占比仅为25%,原研药占比达75%, 创新药的价格接近仿制药的30倍。
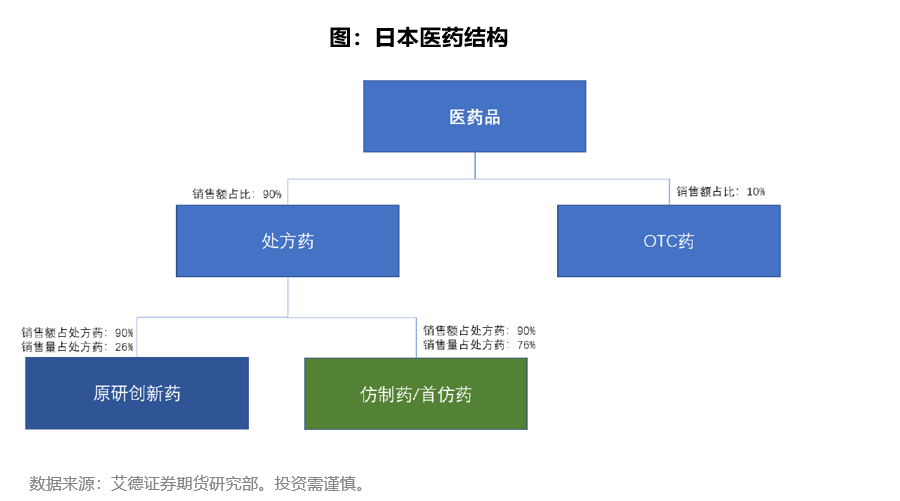
相对日本而言,我国医药结构调整节奏更紧凑,政策执行从研发、生产、销售及税负等多方面往创新药方向倾斜,同时吸引大量早期远赴海外的医药人才返华创业,掀起了创新药研发的热潮。
问题四
国内创新药行业发展现状是怎样的?
答:早年受限于技术、市场、人才、政策等各种因素,国内药企大多以生产仿制药为主,药企依靠仿制或首仿ME-TOO进行发展,研发意识与创新能力淡薄。从新中国成立至2008年,国内一类上市新药仅有5个。
2008年以后国家出台了一系列政策如加强临床试验数据核查、加快创新药审评审批等,全面支持创新药的发展,2009年至2018年,一类上市新药已达20个。到了2018年,已有150余个国产一类新药申报临床,35个一类新药上市,50家以上药企具备基于生物和化学的现代化研发部门,21家企业药品销售额超过百亿元,相较2008年已发生根本性的变化。
(1)从产业需求来看,国内市场规模巨大,拥有超过上亿的65岁以上老龄人口,庞大的基数以及老龄化的加速为创新药带来了巨大的市场,并且需求逐年上升。
(2)从医疗卫生水平来看,国内仍然存在很大的提高空间,目前国内医疗卫生支出占GDP比例为6.2%,人均健康支出为426美元左右,与发达国家相比差距仍然较大,根据国家政策的规划,未来相关指标将向发达国家看齐。
(3)从医疗支付体系来看,我国医疗系统市场化程度较低,主要依靠国家医保进行保障,因此政府对于价格标准制定的参与度较高。
目前,我国创新药行业处于高速发展期,申报的品种数量正在逐年增加。例如2018年新申报的国产新药IND(新药研究申请,新药在被用于人体临床试验之前,申请者必须向FDA递交新药研究申请)数量已经达到300个以上,这些申报的品种预计将于3-5年以后逐步获批上市。
未来,通过人才引进和技术突破等多重利好的落实,中国在创新药研发多个领域与发达国家的差距将逐渐缩小,国内市场每年获批的创新药数量将呈大幅增长态势。
2019年我国创新药市场规模为1325亿美元,在我国制药市场中占比高达56.1%,预计2019年至2021年持续按复合年增长率8.8%增长,到2021年中国创新药市场将突破1500亿美元。
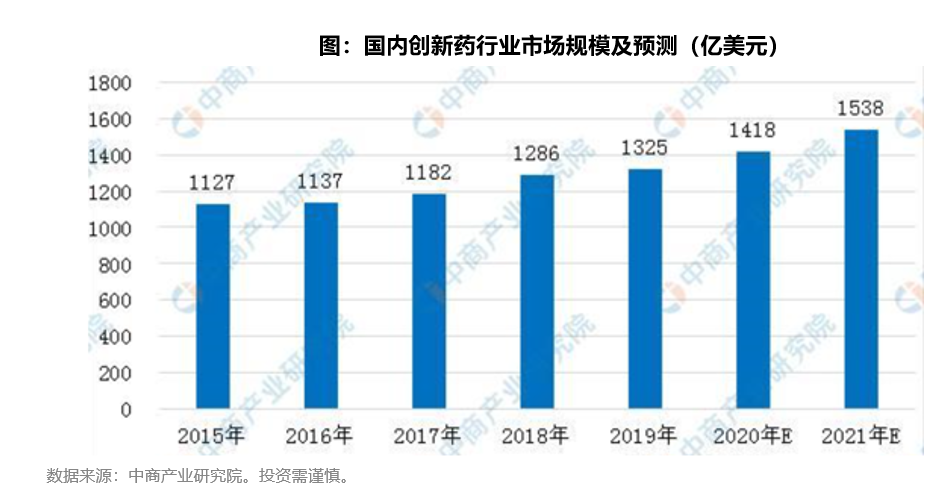
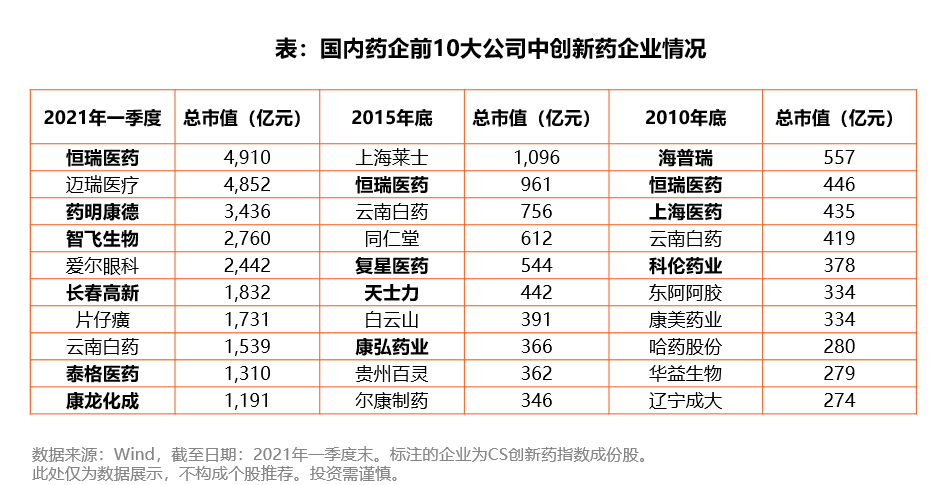
就A股上市公司而言,越来越多的创新药公司成为医药板块的头部企业,目前已有6家创新药公司进入医药板块市值前10大之列。
预计未来市值前10大的药企名单还将进一步变化,还会有更多的拥有创新能力和技术优势的创新药公司进入行列。
问题五
我国发展创新药有何优势?
答:我国企业在全球医药研发金额的占比已经达到了20%,低于美国47%的水平,但超过英国位居第二位。在当前我国医疗需求提升、监管改革深入进行的背景下,未来国内创新药企将迎来发展的黄金窗口期。
(1)中国创新药企业新药研发成本控制领先全球。国内新药研发费用远低于欧美,当前我国获批上市的新药研发费用中值约1亿元,而欧美部分肿瘤新药的研发费用中值为5亿美元。
(2)我国庞大的人口基数为创新药提供了丰富临床资源。创新药在研发过程中需进行多期临床试验,医院是承担临床试验研究的主要机构。2018年美国医院月均就诊人数为493人,而中国高达1259人。在中国开展临床试验可有效缩短招募时间,同时也可以提供更广泛的疾病谱进而提高了临床试验效率,我国PD-1/PD-L1临床患者招募率是美国的6倍;
(3)监管改革持续深入,新药获批速度加快。在药审改革之后,自主新药的报批周期从8年减少到了5年左右,特殊品种报批周期有望压缩到3-4年。另一方面,过程新药临床申请(IND)数量持续爆发,在报批周期缩短的背景下,国产新药每年获批的数量有望进一步增长。
(4)国内创新药企业具有后发优势。目前国内创新药企业主要以跟随式创新为主,免去了在新药研发中失败风险最大的概念验证的环节。即使自主新药上市时间落后外企3-6年,目前国内采用的Me-too替代依然能够顺利实现,这主要是由于在疗效相似的前提下,自主新药的定价更低,以及本土化的营销团队更加专业所致。未来我国自主创新药的市场份额有望持续扩大。
(5)人才优势与工程师红利帮助国内企业更好地投入医药研发。中国理工学科大学毕业人数高居全球首位,中国研究生毕业人数从2003年的2.01万人增长至2018年的51.94万人,留学归国人数也相应的从11.11万人上升至60.44万人。不断增长的国内毕业研究生和留学回国人员源源不断的为国内创新药企业输送大量科研人才,同时相对较低的专业人才薪酬帮助企业以更低的成本进行创新研发。
(6)集采政策帮助境内药企抢占市场份额。不同与境外医疗机构,中国医药下游消费以公立医院为主,在国家医保局常态化集采的政策下,能否进入医保目录对药品的销量至关重要。中国创新药具有成本与政策扶持的双重优势,能够通过进入医保目录大幅提升渗透率。
问题六
未来创新药产业发展有哪些新趋势,哪些领域值得重点关注?
答:可重点关注CXO、肿瘤药和疫苗。
(1)医药外包组织(CRO、CMO及CSO)。CXO解决了创新药企业研发实力不足、营销能力有限以及流通成本居高不下等困境。CRO/CMO头部公司在持续积累下规模化优势、产业链优势不断加强,在提升新药研发效率方面优势明显,例如目前在临床和申报阶段CRO大约可以节约30%左右的时间,这将可能为一款新药在竞争中带来一定的先发优势。CRO/CMO渗透率持续提升将是长期趋势,具备较强的确定性
最近两年由于新冠疫情的影响,对CRO和CMO行业造成一定扰动,收入端增速较过去有所放缓。但影响程度相对有限,相关上市公司均实现正增长,增速主要保持在0-20%区间。
临床前CRO基于实验室,而CMO基于工厂,因此在建工程在一定程度上均反映出CRO/CMO公司对于产能的投入。近两年,基于行业景气度不断提升,订单需求持续加大,各家头部公司在建工程规模保持快速增长的状态。尤其是2020年,大部分公司的在建工程投入未受到疫情影响,相较于2019年呈现出加速的趋势,体现出一方面订单需求仍较为旺盛,在产能较为饱和的情况下需要建设新产能,另一方面体现出各家公司对于行业未来发展前景的信心。
当前,中国CRO市场能实现复合25%以上的增速,远高于全球市场5%-10%的年增长率,一方面来源于中国创新药市场的快速成长,另一方面中国正承接来自全球CRO的产能转移。全球产能转移趋势是我国CRO/CMO成长的重要基石,从当前较多头部公司的收入结构来看,其海外收入占据着较高的比例,且增速均远高于全球市场平均增速。以药明康德为例,其2019年海外收入占比约为77%,2015-2019年复合增长率约为25.6%。
我国能成为全球CRO产能转移重要承接方,工程师红利是重要因素之一。以CRO为例,泰格医药2018年平均人工成本只有16万元/人,而其59%员工位于美国的子公司方达医药平均人工成本达到30万元/人。同年,跨国CRO企业InVentiv Health、ICON以及PRA等平均人工成本分别为97万、55万、55万元,相比之下国内企业人工成本优势显著。
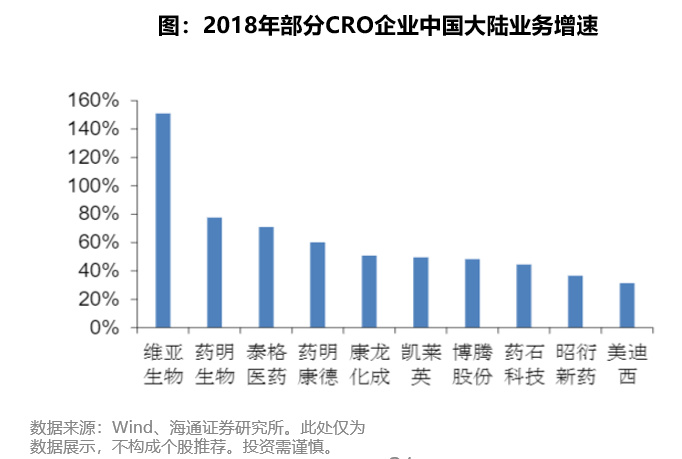
展望未来,全球CRO产业链向中国转移趋势确定性较强,一方面是因为人口红利和工程师红利等优势仍然存在,中国始终是产业链转移的核心选项;另一方面,对比其他潜在国家(例如印度),对于可能会受到影响的临床前CRO和CMO领域,承接全球CRO产业链转移的趋势受到扰动可能性较小。同时国内需求在快速提升,以2018年为例,多家CRO企业中国大陆业务增速超过40%。未来,国内需求将逐步成为我国CRO/CMO行业发展的主要驱动力。
(2)肿瘤药。我国是世界上恶性肿瘤年发病率最高的国家,而且发病率和死亡率均逐年上升。2015年发病中标率为190.64/10万,高于世标率的186.39/10万。随着我国经济的发展,内陆城市空气质量不断下降,短期内,我国肿瘤发病率还将持续高位增长。在疾病发病率和死亡率攀升的压力下,寻求积极有效的创新疗法需求不断增加。
目前国内肿瘤药市场以传统化疗药物为主,生物创新药市场潜力较大。对比2019年全球和国内10大畅销肿瘤药物榜单发现,传统化疗药物已不存在全球10大肿瘤药物之列,而国内的榜单中,该类药物占比仍然有40%。这表明国内抗肿瘤创新药市场可替代空间巨大。同时,2019年全球10大畅销肿瘤药中,生物创新药占比达到60%,而国内榜单中仅有3只是生物药,国内抗肿瘤药物仍然以化学药为主,说明生物创新药在国内市场中发展空间显著。
对比海外发达国家,预后较好的肿瘤5年生存期存在差距,也在驱动抗肿瘤创新药研发。例如2015年我国恶性肿瘤的5年相对生存率为40%左右,较10年前提高10%,但与发达国家相比仍有较大提高空间。
按照医药市场规模测算维度:用药人群+渗透率+时间长短+用药金额,我们认为以下创新药领域值得关注:
1)肺癌,例如PD-1;
2)乳腺癌,例如呲咯替尼;
3)血液肿瘤,例如赞布替尼;
4)糖尿病:例如洛塞那肽;
5)黄斑变性,例如康柏西普;
6)丙肝,例如达诺瑞韦+拉维达韦。
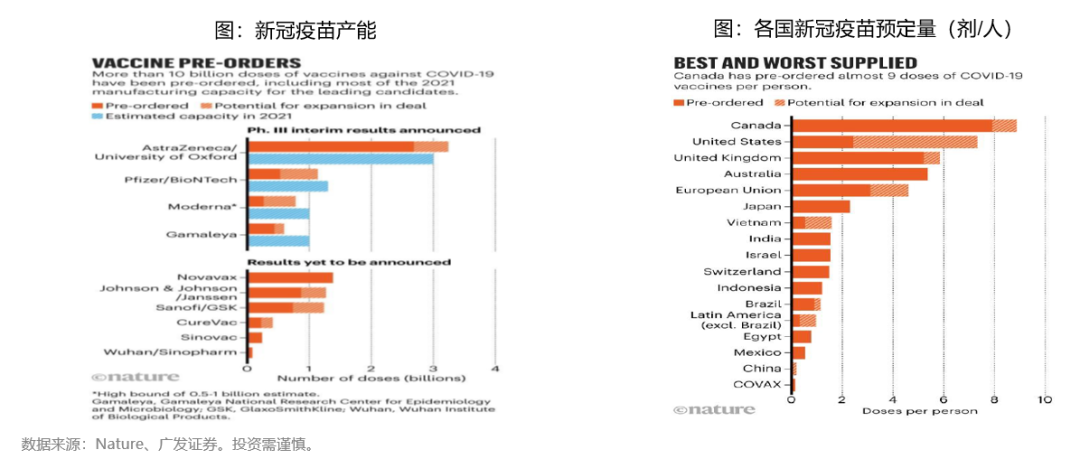
(3)疫苗。全球新冠疫情依然保持严峻,使得市场对疫苗的需求有增无减。截止目前全球新冠疫苗厂商已披露2021年理论产能共计约98亿剂,但在设备、原料、冷链物流等因素的限制下,其产能仍难以满足市场需求;
高收入国家已预定了当前全球约50%的产能,中低收入国家将更加依赖中国产能。目前国内新冠疫苗研发进度处于全球前列,共12个新冠疫苗处于临床开发阶段,明年有望大规模应用于健康人群,预计未来新冠疫苗上市后接种需求旺盛。
问题七
未来创新药行业发展主要驱动因素是哪些方面?
答:国内创新药行业市场规模或将在未来很长一段时间内持续快速增长,我们认为主要受以下几个因素的驱动:
(1)政策利好:国家对于创新药不断给予政策支持,颁布如《关于深化审评审批制度改革鼓励药品医疗器械创新的实施意见》、《关于药品注册审评审批若干政策的公告》等一系列政策,引导医药企业加大研发投入,加速创新药审评、审批及上市的步伐,从上至下推动创新药行业快速发展。从效果上看,相关政策对于新药上市推进效果显著,2019年新药上市申请时间平均用时427天,同比减少50%。
(2)海外人才回流:国内第一批创新药企业多为海归人才参与支持建设,未来随着国际形势转向保守,美国签证收紧等影响,预计将有越来越多的海外创新药人才归国,将为创新药行业带来强大的技术支持。
(3)技术输出:2019年共有11款国产新药在国内获批上市,授权合作案例越来越频繁,同年,国产抗癌药泽步替尼(百济神州生产)在美国上市,国内创新药企业已具备对外技术输出能力。我们认为随着技术基础长期不断积累,未来我国创新药技术输出将呈现高速增长趋势,这将为国内创新药带来新的发展空间。
(4)人口老龄化:我国人口老龄化趋势明显并呈现出加速的状态。据统计,中国老龄化速度远高于全球平均水平,2014年至2019年,我国65岁以上人口增长0.4亿至1.8亿,2019年老龄化人口占总人口的比例已达到12.6%。越来越多的老年人对创新药产业来说意味着越来越大的市场空间,未来创新药的需求将不断加大。
(5)居民医疗支付能力保障:2015年至2019年我国城镇化率从56.1%提升至60.6%,城镇人口的增加带来了城镇医保人口的增多,大家对医疗支出的意识加强,可负担高昂创新药药品费用的人群不断扩大,这些都为创新药支付能力提供了保障。加之医保目录扩容,纳入多种创新药。有助于降低患者支付负担,为创新药提供了市场空间。
(6)金融市场改革:如香港联交所18A和注册制的实施,为更多尚未盈利的创新药企业提供了获得长期融资的机会,使得社会资本市场可以参与创新药行业的投资与发展,为创新药行业提供了更多的资金支持。
(7)国内药企创新转型:国内各类型药企迎合政策利好,纷纷加速转型步伐,通过自主研发、合作研发、收购合并等方式,不断向创新药业务领域深耕。根据《医药经济报》数据,2019年上半年我国研发型药企数量达到301家,远高于2018年底的262家。此外,国内医药研发支出快速增长,2013年至2018年,A股化学制药、生物制药板块合计研发支出从59.6亿迅速增长至242.3亿。未来医药产业特别是创新药板块的研发支出还将不断加速,国内药企创新转型正迈入快速道。